گزارشی از یک تشخیص.
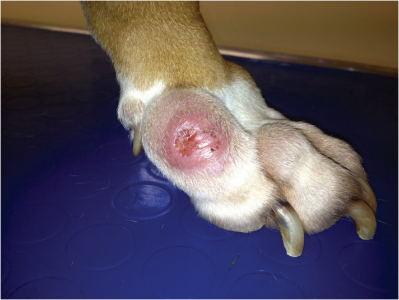
یک سگ باکسر ماده شش ساله با تاریخچه ای 13 ماهه از ضایعات پوستی خارشی متوسط و پیشرونده ارجاع گردیده. سگ فوق بطور متداول مایه کوبی و انگل زدایی شده و با جیره غذایی تجاری خشک پرکیفیت تغذیه می شود. درمانهای قبلی شامل آموکسی سیلین بعلاوه اسید کلاواولانیک (20 میلی گرم برای هر کیلو در هر 12 ساعت) ، سفالکسین(25 میلی گرم برای هر کیلوگرم در هر 12 ساعت) به تنهایی یا آمیخته با پردنیزولون (05 میلی گرم برای هر کیلوگرم در هر 24 ساعت برای یک هفته و سپس هر روز دیگر) برای یک دوره حدوداً 3 تا 4 هفته بوده ، اما منجر به بهبودی نشده. همچنین صاحب سگ گزارش نموده که حیوان بطور متناوب لنگش غیر متحرکی را بر روی پای قدامی سمت راست تجربه می نموده. معاینات فیزیکی سگ متعاقب ورود هیچ اختلالی را نشان نداد. در معاینات پوستی 9 گرهک پوستی زخمی شونده و غیر زخمی مشاهده گردید که ابعاد قطری آنها از 1 تا 7 سانتی متر متغییر بود و اساساً بر روی برجستگی های استخوانی انتهایی دور و انگشتان پاهای قدامی (تصویر 1) ، آرنج چپ، و زانوی راست توزیع شده بود.
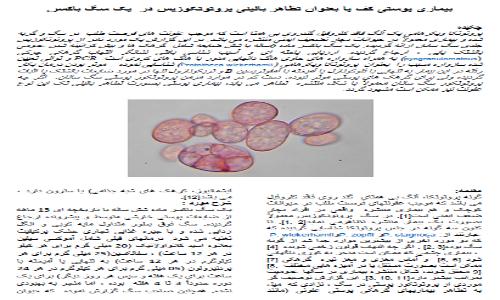
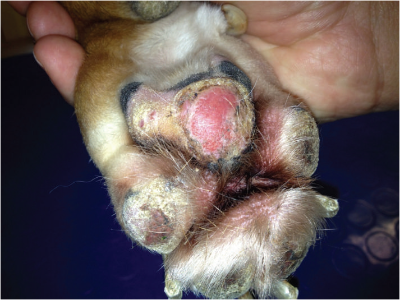
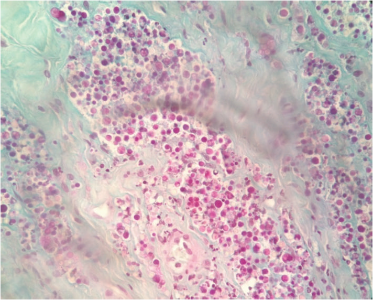
. دیگر ضایعات پوستی شامل بیش کراتینه شده، دلمه بستن ، رنگدانه زدایی و تخریش بالشتک پایی بود (تصویر 2). در آن موقع اصلی ترین تشخیص های تفریقی شامل گرهک های عفونی یا سترون و نودشتاری(نئو پلازی) بود. بررسی یاخته ای در نمونه های اخذ شده از گرهک های پوستی غیر زخمی نشانگر روند التهابی گرهکی چرکی و ریزسازواره های کروی شکل برون یاخته ای بسیار با قطری 20 تا 30 میکرو متری که اغلب حاوی 2 هاگ با قطرحدوداً 10 میکرو متری بوده.
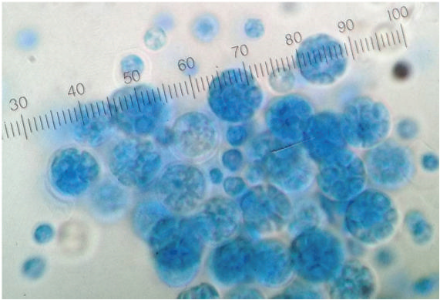
تشخیص اولیه عفونت قارچی عمومی بود. نمونه های اخذ شده از گرهک های غیر زخمی در محیط آزمایشی درماتوفیتی در دمای اطاقی کشت گردیدند. علاوه بر این تکه برداری های پوستی از گرهک های دست نخوره به همراه نمونه های خون و ادرار برای کار های بیشتر آزمایشگاهی و سرم شناسی اخذ گردید(صاحب دام اجازه نمونه گیری از ضایعات بالشتک پا را نداد) . پرتونگاره های سینه ای و شکمی نیز گرفته شد اما جالب توجه نبود. ارزیابی های خون شناسی ، زیست شیمی سرمی، هیچ نوع اختلالی را نشان نداد و سرم شناسی برای تمامی پادتن های لیشمانیا اینفانتوم، ارلیشیا کانیس، و آناپلاسما فاگوسیتوفیلیوم و پادگن های دایروفیلاریا ایمیتیس منفی بود. پس از چهار روز کشت در گرمخانه ، پرگنه های نرم ، کرمی شبه مخمری بر روی محیط های آزمایشی درماتوفیتی رشد نمود. در برسی با ریزبین نوری اسلاید های تهیه شده در لاکتوفنل از این پرگنه ها هاگدانهای مدور حاوی هاگ های کروی مشابه با P. wickerhamii آشکار گردید(تصویر 3).
یاخته های P. zopfii به شکل بیضی یا استوانه ای بوده ، تولید هاگدانهایی با قطر بزرگتر(15-25 میکرومتر) تا محتوای 20 هاگ را می کنند. در مقابل یاخته های P. wickerhamii به شکل مایل به دایره ای بوده(7-13 میکرومتر قطر) ، هاگدانهایی محتوی هاگهای کروی تا 50 عدد را ایجاد می کنند[2]. آسیب شناسی بافتی نشانگر التهاب پوستی والتهاب نیام چربی دار چند گرهکی ، گره دار تا منتشره (با لنفوسیت ها، پلاسما سل ها، یاخته های بیگانه خوار درشت پیکر، و نوتروفیلها) با سازواره های بیشماری از گونه های پروتکا می باشد. به لحاظ ریخت شناسی دیواره این یاخته ها با رنگ آمیزی اسید شیف مرحله ای ارغونی روشن می شود(تصویر 4 ) و اغلب این ریزسازواره ها برون یاخته ای بوده یا منفرد و یا بیشتر گروهی مشاهده شده و تنها تعداد کمی درون یاخته های بیگانه خواره دیده می شوند.
با بکار گیری مینی کیت ها QIAamp و دستورالعمل های محصول فوق حدوداً 1 میلی متر مکعب از ماده کشت برای جداسازی DNA مورد استفاده قرار گرفت. بخشی از ژن RNA ریبوزومی 28S با استفاده از پرایمرهای منتشر شده قبلی تکثیر گردید [13] . نوار ایجاد شده بر روی ژل جدا شده و DNA با استفاده از کیت اسپین آگاروز جدا گردید. DNA جدا شده متعاقباً با پرایمرهای PCR مرتب شده ، PCR یک نوار تقریباً 350pb را ایجاد می نماید.
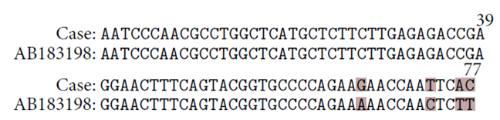
چون تعیین توالی طول کامل محصول PCR ممکن نیست ، یک توالی 77pb با استفاده از پرایمر U2 بدست آمده. درورای آن قطعه اوج های مضاعف نشانگر وجود بیش از یک نژاد است. توالی های مشابه در بانک ژنی با کمک اطلاعات شبکه نرم افزار Blast مورد جستجو قرار گرفت بطوری که 9 مورد از این توالی ها متعلق به سویه های پروتوتکا ویکرهامی بودند؛ بالا ترین تشابه توالی مربوط به ژن بانکی به شماره AB183198 بوده (تصویر 5). این نتیجه تشخیص پروتوتکوز جلدی ناشی از پروتوتکاویکرهامی را تایید نمود. چون هیچ رهنمود درمانی دردست نبود ، بیمار با فلوکونازول خوراکی(10 میلی گرم برای هر کیلو دو بار در روز) تحت درمان قرار گرفت ، بر اساس گزارش ها ترکیباتی احتمالاً در مقابله با گونه های پروتوتکا سودمند تر هستند ، همچون آمفوتریسین B ، فلوکونازول ، ایتراکونازول، و احتمالاً تربینافین[2] . اگر چه بهبودی بالینی قابل توجهی در ضایعات بالشتک پایی پس از یک ماه با فلوکونازول ثبیت شده ، این رژیم درمان به میزان اندکی روند پیشرفت گرهک های پوستی را کند می نماید، زیرا که سازواره پروتوتکا در ارزیابی یاخته ای قابل شناسایی است. وقتی که تجویز فلوکونازول کنار گذاشته شد ، آمفوتریسین B بصورت دو بار در هفته بصورت تزریق زیر جلدی مطابق با آیینگان درمانی برای درمان کریپتوکوکوز سگ سانان استفاده می گردید[14]. بطور اختصاصی ، 0.5 میلی گرم آمفوتریسین B برای هر کیلوگرم بصورت زیر جلدی دو بار در هفته در 500 میلی لیتر از محلول کلرور سدیم 45% دکستروز 2.5% تجویز می گردید. همزمان سگ تحت درمان با ایتراکوناز (5میلی گرم برای هر کیلو بصورت خوراکی یک بار در روز) قرار گرفته، بدلیل سمیت کلیوی آمفوتریسین B پس از 7 تزریق کنار گذاشته شد و بیمار همچنان برای شش ماه تحت درمان با ایتراکونازول قرار گرفت . به هر حال علارغم عدم بهبودی گرهک های پوستی با اعمال این رژیم درمانی بالشتک های پایی تا رسیدن به وضع عادی بسته ماندند.